本道生物公布BTL-203(FcRn抑制剂)临床前PK/PD数据
本道生物今日公布其半衰期延长型新生儿Fc受体(FcRn)抑制剂BTL-203的积极临床前药代动力学/药效学(PK/PD)研究结果。在食蟹猴模型中,单次静脉注射(IV)或皮下注射(SC)BTL-203均能实现总免疫球蛋白G(IgG)的深度且持续降低。
“目前获批的FcRn疗法均需每周给药(皮下)或每两周一次给药(静脉注射)。根据临床前的PK‑PD数据,我们比较有把握地预测,BTL‑203在人体中可以实现每四周一次皮下给药。我们相信这会给患者带来很大的便利性;并且BTL-203会有更优效的IgG降低能力,使BTL‑203有望成为同类最佳的疗法(Best-in-Class),这将在临床研究中进一步验证。”
— 杨见松博士,本道生物首席执行官
非临床研究亮点
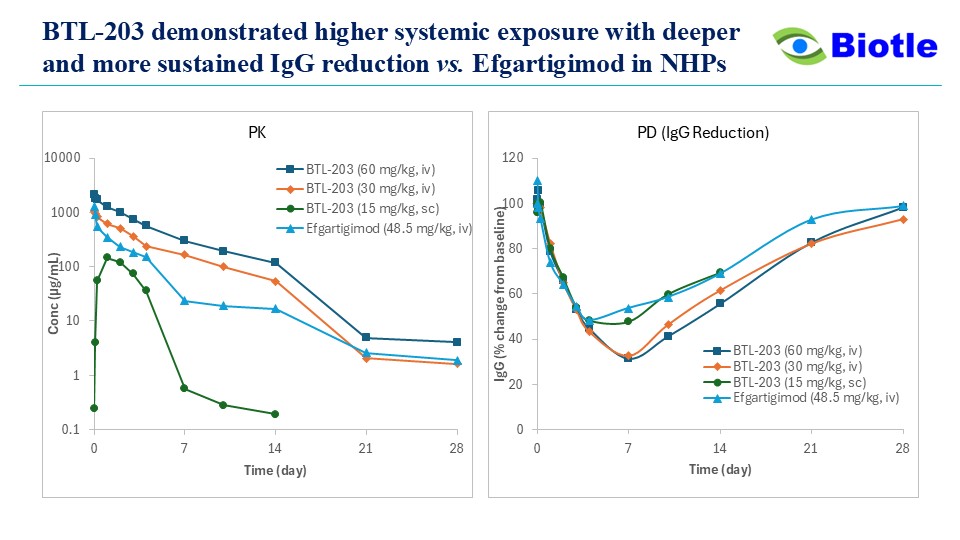
- 相较于对照组的强效IgG降低: 研究中单次静脉注射BTL‑203(60或30 mg/kg)比静脉注射艾加莫德(48.5 mg/kg)具有更高的系统暴露量和更深度、更持久的总IgG降低效果;最低降幅达约67–69%,约4周后恢复。
- 皮下给药: 15 mg/kg皮下给药的BTL‑203可实现与48.5 mg/kg静脉注射艾加莫德相当的IgG降低效果。
- 转化预测: 群体PK/PD模型提示人体四周一次皮下给药可维持目标治疗窗内的IgG降低水平。
- 耐受性与安全性: BTL‑203在食蟹猴中耐受性良好。15 mg/kg皮下给药时,白蛋白降低和LDL‑C变化轻微且可逆。
关于BTL-203
BTL‑203是一种经过工程化设计、具有延长暴露量和低频皮下给药特性的FcRn抑制剂。通过阻断FcRn,BTL‑203可加速IgG分解代谢,这一机制在多种IgG介导的疾病(如重症肌无力、慢性炎症性脱髓鞘性多发性神经病CIDP等)中已得到验证。本道生物正在推进BTL‑203的临床开发(计划于2026年第二季度提交IND申请),并积极寻求合作伙伴以加速全球开发和商业化进程。
商业合作 如需洽谈合作,请联系我们。

